
dr n. med. Nastazja Dagny Pilonis (PIB NIO M. Skłodowskiej-Curie)
Jak zoptymalizować wskaźnik oczyszczenia jelit?
Sesja: jak uniknąć raka jelita grubego po kolonoskopii podczas ESGE Days 2023
Wytyczne ESGE z 2019 roku prowadzą krok po kroku przez proces właściwego przygotowania pacjenta, a mimo to nadal znaczny odsetek kolonoskopii wymaga powtórzenia ze względu na niską jakość oczyszczenia jelita.
Nieodpowiednie przygotowanie do badania to nie tylko dodatkowe koszty i czas związane z koniecznością wielokrotnego powtarzania badania, to także wyższe ryzyko przeoczenia zmian i/lub polipów, niższy odsetek osiągnięcia zastawki kątniczo-krętniczej i wreszcie znaczny spadek tolerancji pacjenta do całej procedury związanej z kolonoskopią.
I tu dr Pilonis stawia pytanie: a więc jak zoptymalizować wskaźnik oczyszczenia jelit?
W odpowiedzi proponuje podział czynników, które wpływają na jakość oczyszczenia jelit na 3 grupy: przed procedurą (kolonoskopią), w trakcie procedury i po zakończeniu badania.
Przed procedurą
Pierwszym omawianym czynnikiem jest stosowanie dawek podzielonych preparatu do oczyszczania jelit. Metaanaliza z 2014 roku, która objęła 29 randomizowanych kontrolowanych badań jasno wykazała, że stosowanie dawek dzielonych jest skuteczniejsze od stosowania dawek jednodniowych (85% vs. 63%)1. Aby w pełni wykorzystać korzyści, które płyną ze stosowania dawek dzielonych należy je traktować jako obowiązkowy element przygotowania. Wyniki badania z 2023 roku pokazują, że kiedy pacjenci nie mieli wyboru i byli przygotowywani modelem split-dose ich przygotowanie jelita oceniano na 90%, podczas gdy pacjenci, którym schemat split-dose był zaproponowany jako jedna z opcji osiągali zaledwie 79%2.
Kolejnym kluczowym czynnikiem jest czas przyjęcia preparatu: zgodnie z wytycznymi ESGE 2019 kolonoskopia powinna się odbyć w ciągu 2-5 godzin po podaniu drugiej dawki preparatu. Wydłużenie tego okresu o każde 4h obniża jakość przygotowania jelit o 10%, więc w sytuacji, kiedy pacjent jest przygotowywany dzień przed badaniem jakość oczyszczenia jelit może spaść nawet do 70%.
Ostatnim z czynników z tej grupy jest edukacja pacjenta. Jest to stara wiadomość, ale cały czas aktualna – rozszerzone informacje dla pacjentów czy to w formie pisemnej, ustnej, w formie filmu lub animacji działają na korzyść lepszego oczyszczenia jelita. Potwierdza to również metaanaliza z 2017 roku, gdzie pacjenci w grupie, która otrzymała rozszerzone informacje (niezależnie od ich sposobu przekazania) byli lepiej przygotowani do badania niż pacjenci, którzy otrzymali standardowe informacje3.
W dobie obecnych innowacji kwestią czasu są narzędzia, które ułatwią pracę endoskopistów i będą szeroko dostępne dla pacjentów – aplikacje wspierane przez sztuczną inteligencję, które pozwolą ocenić stopień przygotowania pacjenta do kolonoskopii na podstawie koloru wydalin. Wyniki testów takiej aplikacji zaprezentowane przez Inaba A. et al. Podczas UEGW 2022 pokazują, że wynik BBPS ≥ 6 osiągnięto u 99,0% pacjentów.
W trakcie procedury
W sytuacji kiedy jelito nie zostało dostatecznie dobrze oczyszczone z pomocą przychodzą tzw. rescue devices – narzędzia, które umożliwiają spłukanie i odessanie resztek stolca podczas już trwającego badania. Neumann zaprezentował wyniki badania stosowania takiego urządzenia na 96 pacjentach – CIR (cecal intubation rate) wyniósł 84,5%, a nieadekwatne przygotowanie jelita zostało zredukowane z 62% do 4% (p<0.001)4.
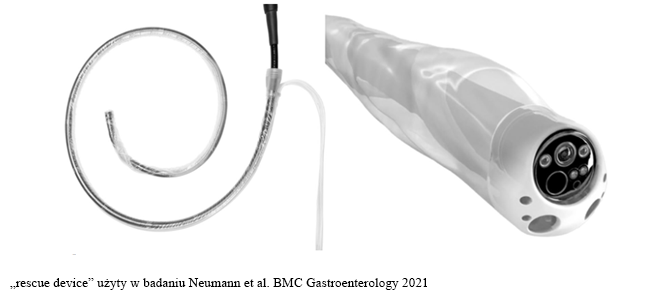
Kolejnym przydanym narzędziem może być ocena oczyszczenia jelita wspomagana przez sztuczną inteligencję i ustandaryzowane raportowanie – oprogramowanie, które w czasie rzeczywistym ocenia wg BBPS stopień oczyszczenia jelita5.
Po zakończeniu procedury
Po zakończeniu badania w przypadku niedostatecznie dobrego oczyszczenia jelita należy podjąć decyzję, kiedy powtórzyć kolonoskopię. Wytyczne mówią, że należy badanie powtórzyć wcześnie, ale co to właściwie oznacza?
Na to pytanie mogą odpowiedzieć wyniki randomizowanego kontrolowanego badania Sanchez et al. Digestive Endoscopy 2022 – 414 pacjentów z niedostatecznie dobrze oczyszczonym jelitem poddano powtórnej kolonoskopii w ciągu średnio 28 dni od pierwszego badania. Odsetek pominiętych zmian – miss rate (95% Cl) – dla gruczolaków wyniósł średnio 68,9%, dla zaawansowanych gruczolaków 60,2%, dla polipów ząbkowanych 83,8% i aż 100% dla raka jelita grubego w prawej części jelita.
- Bucci C et al. Gastrointest Endosc.2014 Oct;80(4):566-576
- Dolovich C. et al. Endoscopy 2023
- Guo X. et al. GIE 2017
- Neumann et al. BMC Gastroenterology 2021
- Zhou et al. Lancet Dig Health 2021
dr Maria Pellisé Urquiza
Polipektomia na zimno – jak uniknąć komplikacji.
Sesja przypadków LGI: nowe podejścia do polipów jelita grubego podczas ESGE Days 2023
85% powikłań endoskopowych jest powiązanych z polipektomią, do których należy odroczone krwawienie, zespół po polipektomii czy odroczona perforacja. Wszystkie te powikłania powstają na skutek użycia diatermii.
Zostało to dobrze udokumentowane w badaniu Suzuki et al. GIE 20181, gdzie podczas kolonoskopii wykonano polipektomię na zimno lub pętlą z diatermią, a następnie oceniono i zmierzono ranę tuż po zabiegu i dzień po zabiegu. Miejsca po usunięciu polipa pętlą na zimno były mniejsze i bez zmian w obrazie śluzówki, podczas gdy blizny po pętli z diatermią były powiększone i owrzodzone. Znaczne różnice zaobserwowano również w głębokości pobranych wycinków, które obejmowały podśluzówkę – dla HSP 81% vs CSP 24%.
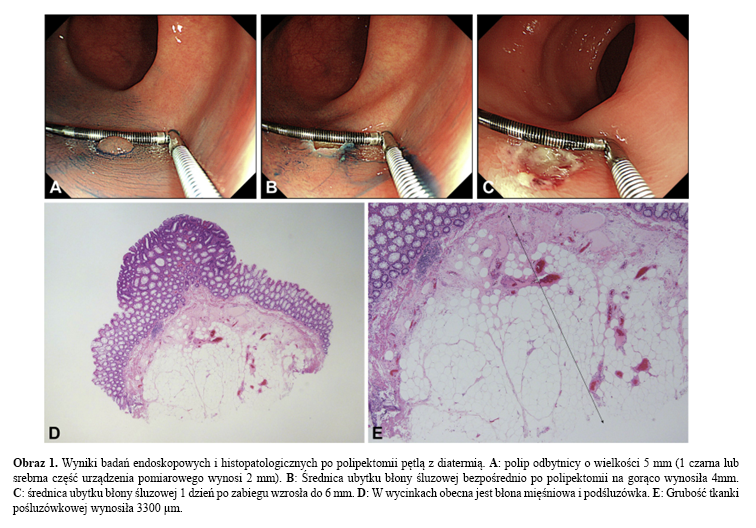
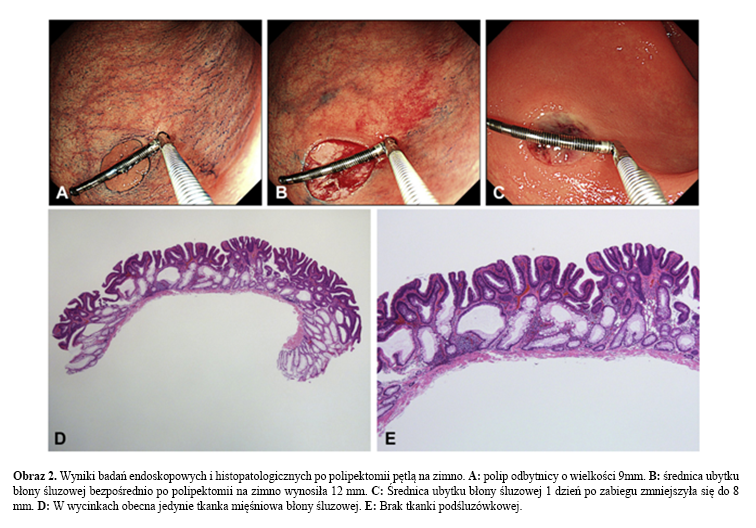
Używając zimnej pętli należy zwrócić szczególną uwagę na:
- zmiany, które przerastają w głąb tkanki podśluzowej,
- odpowiedni margines zdrowej tkanki - należy wziąć większy margines zdrowej tkanki do 1-2 mm – co minimalizuje ryzyko niekompletnej polipektomii (powód rozwinięcia się aż 19-30% raków jelita grubego po kolonoskopii),
- ocenę śluzówki po usunięciu zmiany - bliznę należy przepłukać wodą co pozwoli ocenić czy margines zdrowej tkanki jest odpowiedni. Dodatkowo pojawienie się charakterystycznego „bąbla” świadczy o braku perforacji,
- przy usuwaniu dużych siedzących polipów ząbkowanych należy używać barwnika, żeby oznaczyć granice zmiany i ocenić dokładnie czy nie ma śladów dysplazji,
- technikę pracy: odpowiedni kąt, pozycja na godzinie 6 oraz właściwy dobór pętli.
Różnice w technice dobrze obrazuje grafika pochodząca z publikacji z 2020 roku4: Obraz A - Podczas polipektomii na zimno końcówka endoskopu powinna być skierowana w dół na błonę śluzową, aby umożliwić podcięcie polipa. Obraz B. Odwrotnie jest, gdy stosowana jest diatermia, końcówka endoskopu jest skierowana do światła, obejmując polip, aby zmniejszyć ryzyko głębokiego urazu termicznego.
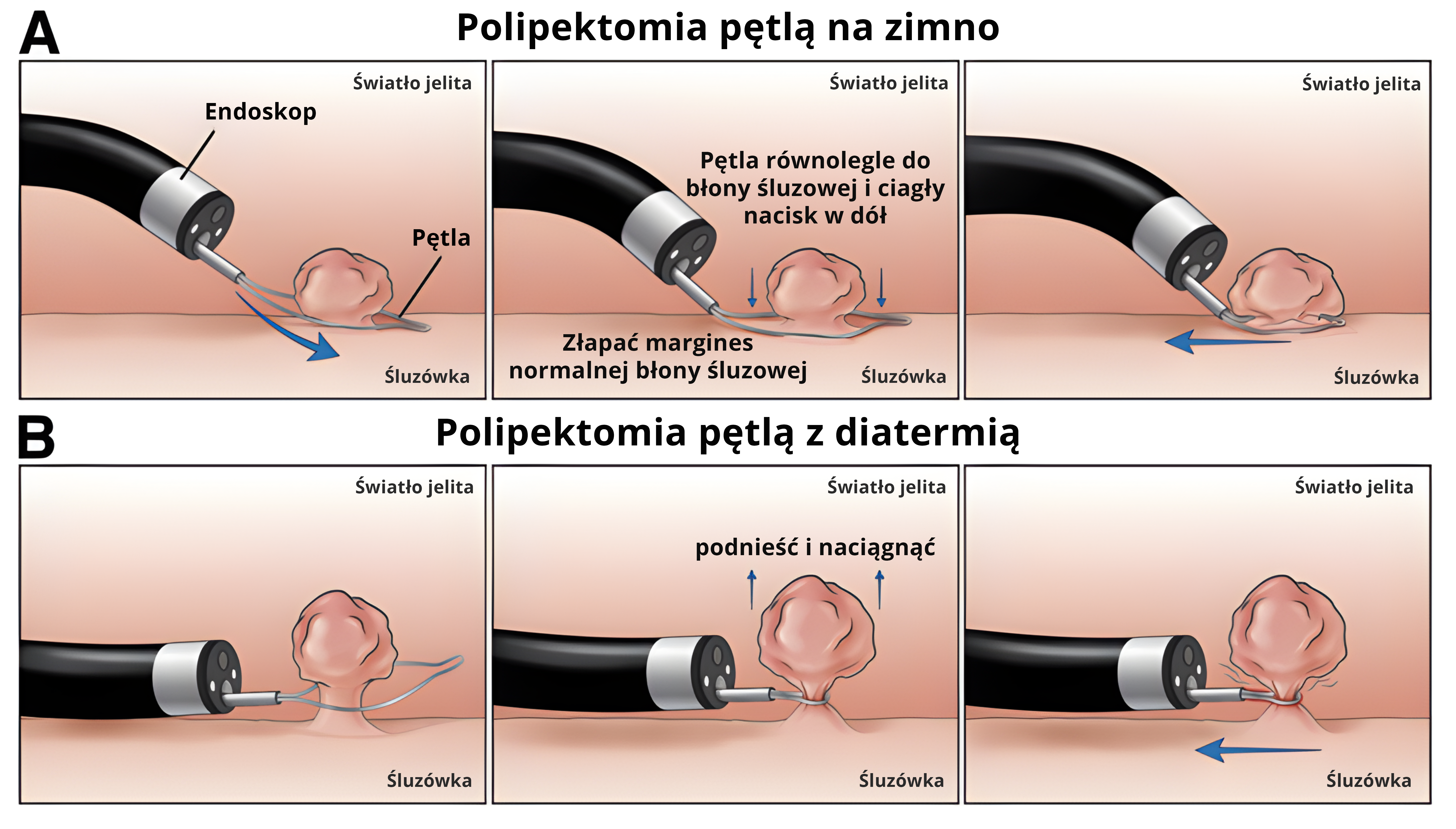
Badanie van Hattem z 20212 wykazało, że częściowa polipektomia na zimno dużych bezszypułowych polipów ząbkowanych jest bezpieczniejsza i równie skuteczna co konwencjonalne EMR, przy jednoczesnym minimalnym ryzyku odroczonego krwawienia czy perforacji. Lektorka, podobnie jak autor wspomnianej publikacji sugerują wprowadzenie do wytycznych częściowej polipektomii na zimno jako techniki pierwszego rzutu przy usuwaniu siedzących polipów ząbkowanych.
Na zakończenie wykładu dr Pellisé wymieniła szereg sytuacji, kiedy użycie zimnej pętli zostało udowodnione jako skuteczne i bezpieczne tj. polipy płaskie i siedzące mniejsze niż 10mm, ząbkowane zmiany siedzące każdej wielkości oraz polipy w dwunastnicy. Natomiast zastosowanie CSP przy polipach uszypułowanych mniejszych niż 10mm, polipach o wielkości 10-20 mm czy gruczolakach powyżej 20 mm nadal niesie ze sobą wiele pytań i wątpliwości, które być może zostaną rozstrzygnięte w przyszłości.
CSP = cold snare polypectomy = polipektomia pętlą na zimno
HSP = hot snare polypectomy = polipektomia pętlą z diatermią
EMR = endoscopic mucosal resection = Mukozektomia endoskopowa
- Suzuki et al. GIE 2018 Width and depth of resection for small colorectal polyps: hot versus cold snare polypectomy
- van Hattem WA, et al. Gut 2021;70:1691–1697. Piecemeal cold snare polypectomy versus conventional endoscopic mucosal resection for large sessile serrated lesions
- Rutter M. Jover R. Personalizing Polypectomy Techniques Based on Polyp Characteristics. Clinical Gastroenterology and Hepatology 2020;18:2859–2867







